快报道
安旭生物IPO前被处理 临床试验数据无法溯源真实性存疑
存在临床试验造假行为,并对其进行处罚。
作者:兮木
来源:GPLP犀牛财经(ID:gplpcn)
1月15日,国家药监局发布关于2020年医疗器械临床试验监督抽查中真实性问题的公告(2021年第11号),点名杭州安旭生物科技股份有限公司(下称“安旭生物”)存在临床试验造假行为,并对其进行处罚。
公告称,国家药品监督管理局于2020年11月,对在审的10个医疗器械注册申请项目开展了临床试验监督抽查,涉及27家临床试验机构,安旭生物赫然在列。
国家药监局发现,安旭生物生产的人类免疫缺陷病毒抗体/丙型肝炎病毒抗体/乙型肝炎病毒表面抗原/梅毒螺旋体抗体联合检测试剂盒(免疫层析法)(受理号:CSZ2000162)在浙江大学医学院附属第一医院开展临床试验中,医疗机构留档的电子照片拍摄时间、地点与临床试验实际时间、地点不一致,临床试验数据无法溯源。
国家药监局决定对该注册申请项目不予注册,并自不予注册之日起1年内不予再次受理该项目的注册申请。
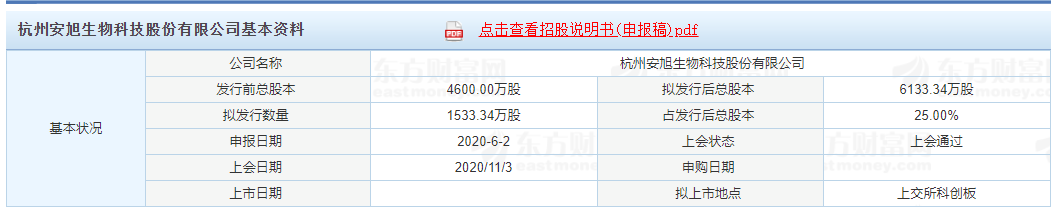
值得注意的是,安旭生物是一家拟科创板上市公司。据悉,2020年6月2日,安旭生物科创板上市申请获受理,拟募资4.59亿元;2020年11月3日,安旭生物通过上市委会议;2020年12月30日,提交科创板注册,目前正在等待注册结果。
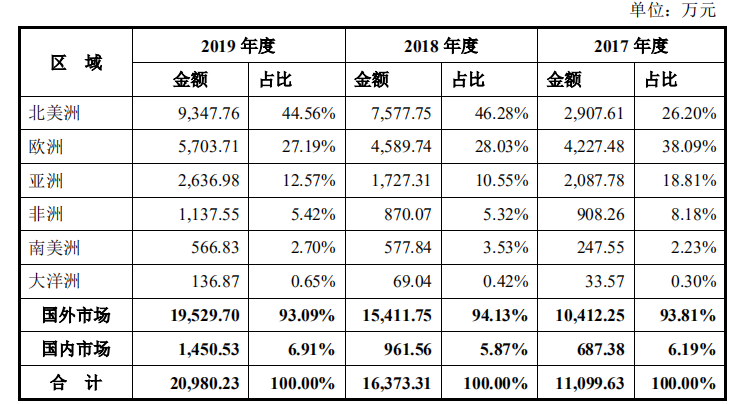
安旭生物招股书显示,其主营POCT试剂及仪器,涵盖毒品检测系列、传染病检测系列等8大类,产品销售以外销为主,2017-2019年,安旭生物的境外收入分别为1.04亿元、1.54亿元、1.95亿元,占总营收的比例分别为93.81%、94.13%、93.09%。总的来看,其境外销售收入占比均超过93%。
(本文仅供参考,不构成投资建议,据此操作风险自担)







You must be logged in to post a comment Login